Este blog tem o objetivo de servir como um complemento ao estudo de uma Disciplina que, historicamente, representa a "alma" da humanidade e de tudo o que existe na Natureza: a QUÍMICA. Em especial, dedico aos meus educandos que, de uma maneira geral, estejam interessados em vencer as barreiras tradicionais da Educação. Abrações.
sábado, 20 de outubro de 2012
quinta-feira, 11 de outubro de 2012
sexta-feira, 5 de outubro de 2012
domingo, 2 de setembro de 2012
Turmas 101 e 102: Dicas para o teste sobre NÚMERO DE OXIDAÇÃO.
ATENÇÃO! Os termos OXIDAÇÃO e REDUÇÃO que aparecem no 2º vídeo não são conteúdo explícito de nosso teste. Atenha-se ao cálculo do número de oxidação, mesmo os compostos sendo participantes de uma reação química. Abrações.
sexta-feira, 31 de agosto de 2012
Turmas 101 e 102: Slides sobre ÁCIDOS e BASES
Para acessar os slides, clica aqui.
Lembrando que os vídeos não poderão ser vistos no slide. Abrações.
Lembrando que os vídeos não poderão ser vistos no slide. Abrações.
quinta-feira, 23 de agosto de 2012
Turmas 91 e 92: Distribuição eletrônica
Pessoal, aqui temos um vídeo explicativo com o conteúdo que foi trabalhado no dia 21/08 (terça-feira à tarde), para os 9ºs anos. Aproveite para revisar! Abraços.
segunda-feira, 30 de julho de 2012
Lista de Exercícios nº 5
Lista de exercícios englobando os conteúdos GEOMETRIA MOLECULAR, POLARIDADE DE LIGAÇÕES, POLARIDADE DE MOLÉCULAS e FORÇAS INTERMOLECULARES: clica aqui.
Abrações.
Abrações.
domingo, 29 de julho de 2012
Teias de aranhas: Biomateriais
As TEIAS de ARANHAS são conhecidas como o mais RESISTENTE dos BIOMATERIAIS.
Todavia, uma questão estava sem resposta: como uma solução protéica, dentro da aranha, se transforma numa fibra tão forte, onde as cadeias estão entrelaçadas e covalentemente unidas entre si?
A resposta apareceu em artigo INÉDITO desta semana: um grupo de químicos descobriu que, quando em solução nas glândulas da aranha, os polipeptídeos tem os grupos funcionais protegidos por grupos protetores inertes, que impedem a adesão intermolecular e fazem com que as proteínas se comportem como globulinas, enoveladas.
Mas, ao serem expelidas pelas glândulas, a solução recebe um suco de reagentes que clivam estes grupos protetores, ativam os grupos funcionais, e o processo de desnovelamento, adesão e construção da fibra ocorre espontaneamente.
Veja artigo COMPLETO GRÁTIS: aqui.
domingo, 22 de julho de 2012
Descoberto novo tipo de ligação química no espaço
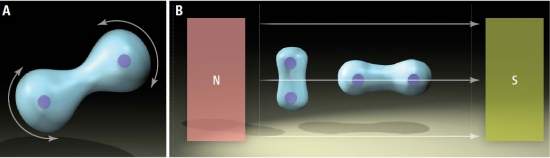
Um fenômeno que aqui na Terra significaria a quebra imediata de uma molécula, nas condições extremas do espaço serve para manter juntos dois átomos, formando uma "molécula magnética". [Imagem: Lange et al./Science]
Cientistas descobriram a possibilidade de um novo tipo de ligação química, mantida por campos magnéticos extremamente fortes.
A reação não poderia ocorrer nas condições naturais da Terra e nem mesmo do Sistema Solar inteiro: ela só ocorre nas proximidades de estrelas de nêutrons ou anãs brancas.
Na Terra, os átomos se ligam por ligações covalentes, ou ligações de hidrogênio - quando eles compartilham elétrons - ou por ligações iônicas - quando a atração eletrostática faz com que íons de cargas opostas se juntem.
No novo tipo de ligação, que Kai Lange e seus colegas da Universidade de Oslo, na Noruega, chamaram de ligação paramagnética, é o magnetismo que mantém os átomos coesos.
Para mais informações, clica aqui.
sexta-feira, 6 de julho de 2012
Lista de exercícios sobre GEOMETRIA MOLECULAR
Para acessar a lista nº 4, sobre Geometria Molecular, clica aqui.
Não esquecer as datas do próximo teste:
TURMA 101: 14/07/2012
TURMA 102: 13/07/2012
Os conteúdos serão os seguintes:
Não esquecer as datas do próximo teste:
TURMA 101: 14/07/2012
TURMA 102: 13/07/2012
Os conteúdos serão os seguintes:
- Ligação Iônica (capítulo 13)
- Ligação Covalente (capítulo 14)
- Ligação Metálica (capítulo 15)
- Geometria Molecular (capítulo 16)
- Listas de exercícios nº 3 e 4.
Abaixo estão alguns vídeos para auxiliar o seu estudo:
Ligações Químicas - Parte 1 - 2
Ligações Químicas - Parte 2 - 2
Geometria Molecular
sábado, 23 de junho de 2012
Lista 3 de exercícios - LIGAÇÕES QUÍMICAS
Lista de exercícios (para as turmas 101 e 102) sobre LIGAÇÕES QUÍMICAS (iônica, covalente e metálica)
Clique aqui (a senha é a mesma já passada em aula).
TRAZER ESSA LISTA DE EXERCÍCIOS NAS AULAS, A PARTIR DO DIA 30/06/2012.
Abraços e muita Luz para todos.
Clique aqui (a senha é a mesma já passada em aula).
TRAZER ESSA LISTA DE EXERCÍCIOS NAS AULAS, A PARTIR DO DIA 30/06/2012.
Abraços e muita Luz para todos.
Vídeo da aula de sábado (23/06/2012)
Olá, meu educandos iluminados. Aqui está o link do Filme QUÍMICA: UMA HISTÓRIA VOLÁTIL (EPISÓDIO 2), passado para as turmas 101 e 102.
http://www.4shared.com/video/DAhtKeWa/Qumica-_Uma_Histria_Voltil_E2-.htm
Aos educandos que estavam viajando, recomendo-lhes assistir ao filme, anotando detalhadamente as principais informações. Assim como aulas experimentais, tudo aquilo que é visto ou comentado em aula é conteúdo de testes e provas.
Abrações a todos.
http://www.4shared.com/video/DAhtKeWa/Qumica-_Uma_Histria_Voltil_E2-.htm
Aos educandos que estavam viajando, recomendo-lhes assistir ao filme, anotando detalhadamente as principais informações. Assim como aulas experimentais, tudo aquilo que é visto ou comentado em aula é conteúdo de testes e provas.
Abrações a todos.
sábado, 2 de junho de 2012
101 e 102 Dicas para o teste!
ATENÇÃO! Não serão permitidos durante o teste:
1- empréstimo de materiais (lápis, borracha, caneta, corretivo, etc);
2- idas ao banheiro ou ao bebedouro;
3- escutar música (durante ou depois do teste).
Pessoas! Para ambas as turmas (101 e 102), abaixo estão as relações de conteúdos e saberes necessários para a satisfatória realização de nosso primeiro teste; lembrando que os testes das duas turmas NÃO são iguais. Outra observação é que há conteúdos implícitos, que não necessariamente estarão expostos aqui, mas que estão contidos nos capítulos do teste (capítulos 9, 10, 11 e 12) e no caderno.
--> Propriedades periódicas: saber os sentidos de crescimento de cada propriedade, bem como as suas relações entre si; saber equacionar reações que envolvam Energia de Ionização e Afinidade Eletrônica; interpretar gráficos (vistos em aula).
--> Tabela Periódica: classificações (representativos, transição); nomes dos grupos. HAVERÁ UMA TABELA PERIÓDICA NO TESTE, PARA CONSULTA OBRIGATÓRIA EM ALGUMAS QUESTÕES.
--> Modelos atômicos: além dos modelos tradicionais (Dalton, Thompson, Rutherford, Bohr e Sommerfield), saber os modelos mais atuais (Heisemberg, De Broglie e Shöredinger).
--> Distribuição Eletrônica: o estudante deverá decorar o diagrama de Linus Pauling, e saber fazer as distribuições em subníveis (s, p, d, f) e em orbitais ("quadradinhos") para átomos neutros e íons. CUIDAR as exceções.
--> Todas as atividades realizadas em sala de aula, e também no laboratório de Química, serão consideradas integrantes do processo avaliativo pelo professor.
--> Alguns conceitos ensinados pela professora anterior serão necessários em algumas questões, tais como: isótopos, isóbaros, isótonos, isoeletrônicos, número atômico, número de massa (A = Z + N).
Abaixo estão alguns vídeos complementares ao estudo:
1- empréstimo de materiais (lápis, borracha, caneta, corretivo, etc);
2- idas ao banheiro ou ao bebedouro;
3- escutar música (durante ou depois do teste).
Pessoas! Para ambas as turmas (101 e 102), abaixo estão as relações de conteúdos e saberes necessários para a satisfatória realização de nosso primeiro teste; lembrando que os testes das duas turmas NÃO são iguais. Outra observação é que há conteúdos implícitos, que não necessariamente estarão expostos aqui, mas que estão contidos nos capítulos do teste (capítulos 9, 10, 11 e 12) e no caderno.
--> Propriedades periódicas: saber os sentidos de crescimento de cada propriedade, bem como as suas relações entre si; saber equacionar reações que envolvam Energia de Ionização e Afinidade Eletrônica; interpretar gráficos (vistos em aula).
--> Tabela Periódica: classificações (representativos, transição); nomes dos grupos. HAVERÁ UMA TABELA PERIÓDICA NO TESTE, PARA CONSULTA OBRIGATÓRIA EM ALGUMAS QUESTÕES.
--> Modelos atômicos: além dos modelos tradicionais (Dalton, Thompson, Rutherford, Bohr e Sommerfield), saber os modelos mais atuais (Heisemberg, De Broglie e Shöredinger).
--> Distribuição Eletrônica: o estudante deverá decorar o diagrama de Linus Pauling, e saber fazer as distribuições em subníveis (s, p, d, f) e em orbitais ("quadradinhos") para átomos neutros e íons. CUIDAR as exceções.
--> Todas as atividades realizadas em sala de aula, e também no laboratório de Química, serão consideradas integrantes do processo avaliativo pelo professor.
--> Alguns conceitos ensinados pela professora anterior serão necessários em algumas questões, tais como: isótopos, isóbaros, isótonos, isoeletrônicos, número atômico, número de massa (A = Z + N).
Abaixo estão alguns vídeos complementares ao estudo:
BONS ESTUDOS! ABRAÇÕES.
sábado, 26 de maio de 2012
Exercícios Complementares
ATENÇÃO, turmas 101 e 102 do CCM: a data de nosso 1º teste do 2º trimestre já foi marcada:
Turma 101: 16/06/2012
Turma 102: 15/06/2012
Os conteúdos, para as duas turmas, serão todos os explicados até o dia 02/06/2012.(Modelos Atômicos, Tabela Periódica, Distribuição Eletrônica, Distribuição em Orbitais e Propriedades Periódicas).
Abaixo, estão listas de exercícios complementares ao vosso estudo (a primeira lista já foi distribuída em aula):
Lista 1 (Modelos Atômicos, Tabela Periódica, Distribuição)
Lista 2 (Propriedades Periódicas)
É NECESSÁRIA UMA SENHA PARA BAIXAR OS ARQUIVOS, QUE SERÁ DADA PELO PROFESSOR EM DIA LETIVO.
Os gabaritos serão fornecidos em aula. Abrações.
Turma 101: 16/06/2012
Turma 102: 15/06/2012
Os conteúdos, para as duas turmas, serão todos os explicados até o dia 02/06/2012.(Modelos Atômicos, Tabela Periódica, Distribuição Eletrônica, Distribuição em Orbitais e Propriedades Periódicas).
Abaixo, estão listas de exercícios complementares ao vosso estudo (a primeira lista já foi distribuída em aula):
Lista 1 (Modelos Atômicos, Tabela Periódica, Distribuição)
Lista 2 (Propriedades Periódicas)
É NECESSÁRIA UMA SENHA PARA BAIXAR OS ARQUIVOS, QUE SERÁ DADA PELO PROFESSOR EM DIA LETIVO.
Os gabaritos serão fornecidos em aula. Abrações.
Assinar:
Postagens (Atom)